Репропорционирование (конпропорционирование, контрдиспропорционирование) — реакции, в которых из двух различных степеней окисления одного и того же элемента получается одна степень окисления: HOCL + HCl → H2O + Cl2
Роль среды в ОВР
Для осуществления заданной окислительно-восстановительной реакции и более глубокого ее протекания необходима определенная кислотность раствора. Выбор среды (кислой или щелочной) можно сделать путем сравнения стандартной ЭДС реакций в кислой и щелочной средах. Оптимальной является та, в которой достигается большее значение ЭДС.
Источник: studopedia.ru
Существует множество классификаций реакций по разным признакам. Одним из них является изменение степеней окисления элементов в ходе реакции. Если это присутствует, то такую реакцию относят к окислительно-восстановительным.
Элементы ОВР
Изменение степеней окисления в ОВР происходит за счёт переноса электронов от одного атома к другому. Атом, отдающий электроны – восстановитель. Атом, принимающий электроны – окислитель. Процессы перехода электронов также имеют названия. Приём электронов – восстановление, отдача электронов – окисление.
ОВР Шоу: Бизнес встреча

Для лучшего понимания ОВР рассмотрим её пример. Это реакция растворения серы в концентрированной азотной кислоте:
Сначала возьмём серу. У неё степень окисления меняется с 0 до +6, значит, она отдаёт электроны и является восстановителем. В реакции происходит окисление серы. Это отражает выражение:
Далее нужно рассмотреть азот. Его степень окисления меняется с +5 до +4, значит, он получает электроны. Следовательно, азотная кислота является окислителем. Происходит восстановление азота:
Виды ОВР
Для большего порядка ОВР решили разбивать на группы.
Межмолекулярные
Этот вид ОВР самый распространённый. В таких реакциях молекулы окислителя и восстановителя разные и в процессах окисления и восстановления участвуют атомы разных элементов.
Примером межмолекулярной ОВР является взаимодействие соляной кислоты с цинком:
Zn 0 + 2H +1 Cl = Zn +2 Cl2 + H2 0 .
Внутримолекулярные
В таких ОВР окислителем и восстановителем является одна и та же молекула.
Например, к таким реакциям относится разложение нитрата натрия.
В этих реакциях атомы одного и того же элемента принимают и отдают электроны.
Одно из таких превращений – пропускание хлора через холодный раствор гидроксида калия.
Cl 0 2 + 2KOH = KCl -1 + KCl +1 O + H2O
Методы уравнивания ОВР
Как и любые другие реакции, ОВР требуют подбора правильных коэффициентов. Это не так просто сделать, как кажется на первый взгляд. Однако существует два способа уравнивания ОВР, которые будут рассмотрены в этом разделе.
Электронный баланс
Метод электронного баланса используется чаще всего. Ниже приведён алгоритм уравнивания реакции таким способом. Параллельно будет уравниваться реакция.
ОВР Шоу: Квартира в новостройке (ДО/ПОСЛЕ)
- Написать уравнение.
Возьмём реакцию фосфина с перманганатом калия, подкисленным серной кислотой:
- Определить элементы, меняющие свою степень окисления.
- Составить уравнения электронного баланса.
- Найти НОК (наименьшее общее кратное) числа передаваемых электронов.
НОК – наименьшее число, делящиеся на взятые числа.
- Разделить НОК на каждый коэффициент перед электроном.
| 5 | P -3 – 8ē = P +5
| 8 | Mn +7 + 5ē = Mn +2
- Написать полученные коэффициенты перед веществами с данными элементами.
- Проверить коэффициенты по всем элементам, участвующим в реакции.
Проверять правильность расстановки коэффициентов следует по такой последовательности элементов: металлы -> неметаллы -> водород -> кислород.
В результате проверки были добавлены коэффициенты перед серной кислотой и водой. Теперь уравнение имеет вид:
- Сделать повторную проверку коэффициентов.
Повторная проверка показала, что коэффициенты расставлены правильно, значит, реакция уравнена.
Электронно-ионный метод
Электронно-ионный метод применим только для реакций, протекающих в растворах в кислой или щелочной среде. Рассмотрим ту же реакцию, но уравняем её другим способом. Также возьмём реакцию фосфина с перманганатом и гидроксидом калия.
- Написать реакцию.
- Определить элементы, меняющие свою степень окисления.
- Определить среду реакции.
В первой реакции среди реагентов есть серная кислота, а среди продуктов ортофосфорная, значит, среда кислая.
Во второй реакции одним из реагентов является гидроксид калия, поэтому среда щелочная.
- Составить уравнения полуреакций.
При разных средах уравнивание реакций происходит по-разному.
-
В кислой среде добавляются H + и H2O. Протон добавляется в части с избытком кислорода, а вода – с недостатком.
MnO4 — + 8H + + 5ē = Mn 2+ + 4H2O
- В щелочной среде прибавляются OH — и H2O. Гидроксогруппу пишут в части с недостатком кислорода, а воду – с избытком.
MnO4 — + 8H + + 5ē = Mn 2+ + 4H2O
| MnO4 — + 8H + + 5ē = Mn 2+ + 4H2O
- Поделить НОК на коэффициенты перед электронами.
| 8 | MnO4 — + 8H + + 5ē = Mn 2+ + 4H2O
- Соединить уравнения полуреакций.
- Сократить повторяющиеся частицы.
5PH3 + 8MnO4 — + 24H + = 15H + + 5PO4 3- + 8Mn 2+ + 12H2O.
- Дописать полное уравнение с разделением электролитов на ионы.
5PH3 + 8K + + 8MnO4 — + 24H + + 12SO4 2- = 15H + + 5PO4 3- + 8Mn 2+ + 8K + + 12SO4 2- + 12H2O.
- Проверить правильность коэффициентов.
В нашем случае коэффициенты поставлены верно, поэтому перейдём к следующему шагу.
- Переписать уравнения в молекулярном виде с коэффициентами.
- Повторно проверить, правильно ли расставлены коэффициенты.
Коэффициенты поставлены верно, следовательно, реакции уравнены.
Значение методов постановки коэффициентов в ОВР
Кажется, что метод электронного баланса проще электронно-ионного метода, однако последний экономит время, так как благодаря ему не нужно подбирать коэффициенты для уравнивания атомов водорода и кислорода, так как это уже сделано при составлении уравнений электронно-ионного баланса. Конечно, такой метод используется только при наличии ионов в реакции. Преимущество по универсальности имеет метод электронного баланса.
Стандартный электродный потенциал системы
Окислительно-восстановительный потенциал (ОВП), или электродный потенциал – показатель способности данного элемента присоединять электроны. Эта величина измеряется в микровольтах (мВ). Чем выше значение ОВП, тем лучше вещество принимает электроны.
ОВП даёт большое представление об окислительно-восстановительных свойствах элементов.
Ряд стандартных электродных потенциалов
Электрохимический ряд напряжения металлов, или ряд стандартных электродных потенциалов, – ряд, который позволяет сравнить окислительно-восстановительные свойства элементов-металлов относительно друг друга. Чем левее стоит элемент, тем лучше он отдаёт электроны. Чем правее находится элемент, тем лучше он принимает электроны.
Ряд напряжения металлов в некоторых моментах не согласуется с Периодическим законом. Это объясняется многими факторами: радиусы элементов, их заряд, число электронов на внешнем электронном уровне и так далее.
Диаграмма Пурбе
Чтобы определить, в каком состоянии находится элемент при данном pH и электродном потенциале системы, используется диаграмма Пурбе. Она даёт полное представление об окислительно-восстановительных свойствах элементов.
В основном диаграмма Пурбе нужна для определения продуктов ОВР. В некоторых реакциях образуется их смесь, а в каких-то при разных условиях могут образоваться разные продукты. Диаграмма Пурбе обобщает их, учитывая электродный потенциал системы и pH раствора, поэтому так окислительно-восстановительные свойства элементов представлены наглядно и лучше понимаются.
ОВР в окружающей среде
Существует множество примеров окислительно-восстановительных реакций вокруг человека.
- Дыхание живых организмов и биохимические реакции. Кислород, поступивший в результате этого процесса, используется для множества биохимических реакций, происходящих в организме. Многие из них относятся к ОВР.
- Горение топлива. Это очень важная ОВР, так как она используется в технических нуждах. Например, для движения транспортных средств, ракет и так далее.
Коррозия металлов

Коррозия металлов – процесс окисления металла в течение некоторого времени.
Виды коррозии
Различают несколько видов коррозии.
Химическая
Этот вид коррозии возникает в результате взаимодействия металла с газом или жидкостью при высокой температуре. Обычно химическая коррозия наблюдается на воздухе, потому что в нём содержится кислород O2 – очень сильный окислитель.
В результате образуется оксид металла, который легче реагирует с водой, поэтому далее происходит взаимодействие поверхности материала с влагой воздуха. Образуется гидроксид металла. На этом этапе коррозия заканчивается.
Электрохимическая
Электрохимическая коррозия – разрушение металла с использованием электрического тока. Процесс коррозии начинается с соприкосновения анода и катода, каждый из которых – металл. Коррозии подвергается металл, у которого значение ОВП меньше, чем у другого металла.
При электрохимической коррозии могут образовываться разные продукты. Это зависит от pH, наличия других ионов в растворе, температуры, давления, длительности процесса и других факторов.
Способы защиты от коррозии
Коррозия – процесс, который наносит вред некоторым веществам, поэтому разрабатываются способы борьбы с ней. Ниже приведены существующие методы устранения коррозии.
Источник: dzodzo.ru
Окислительно-восстановительные реакции

Разбираться в ОВР важно, чтобы хорошо сдать ЕГЭ по химии. Какие реакции называются окислительно-восстановительными, их типы, а также примеры окислителей и восстановителей — в нашей подробной статье.
28 декабря 2021
· Обновлено 3 июня 2022
Что такое ОВР
Окислительно-восстановительная реакция (ОВР) — это реакция, которая протекает с изменением степеней окисления.
В такой реакции всегда участвуют вещество-окислитель и вещество-восстановитель. Другие вещества могут выступать в качестве среды, в которой протекает данная реакция.
Конечно, в каждом правиле есть исключения. Например, реакция диспропорционирования галогенов в горячем растворе щелочи выглядит так: Br2 + KOH = KBrO3 + KBr + H2O. Здесь и окислителем, и восстановителем является простое вещество бром (Br2).
Теперь посмотрим внимательнее на вещества — участники окислительно-восстановительных реакций.
Окислитель — вещество, в состав которого входит ион или атом, который в процессе реакции будет принимать электроны, тем самым понижая свою степень окисления.
Восстановитель — вещество, в состав которого входит ион или атом, который в процессе реакции будет отдавать электроны, тем самым повышая свою степень окисления.
Из определений понятно, что реакция включает два противоположных по действиям явления: процесс окисления и процесс восстановления. Процесс восстановления — это процесс принятия электронов, а процесс окисления — процесс отдачи электронов. Оба процесса протекают одновременно: окислитель восстанавливается, а восстановитель окисляется.
Вот мы и узнали общие закономерности протекания окислительно-восстановительных реакций. Теперь давайте разберемся, какие вещества могут быть окислителями, а какие — восстановителями, и может ли одно вещество проявлять те и другие свойства.
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков

Примеры веществ-окислителей
Только окислителями могут быть элементы в высшей своей степени окисления. Например, S +6 в серной кислоте (H2SO4), N +5 в азотной кислоте (HNO3) или солях-нитратах, Cr +6 в хроматах (CrO4 2− ) и дихроматах (Cr2O7 2− ) соответственно, а также Mn +7 (MnO 4− ).
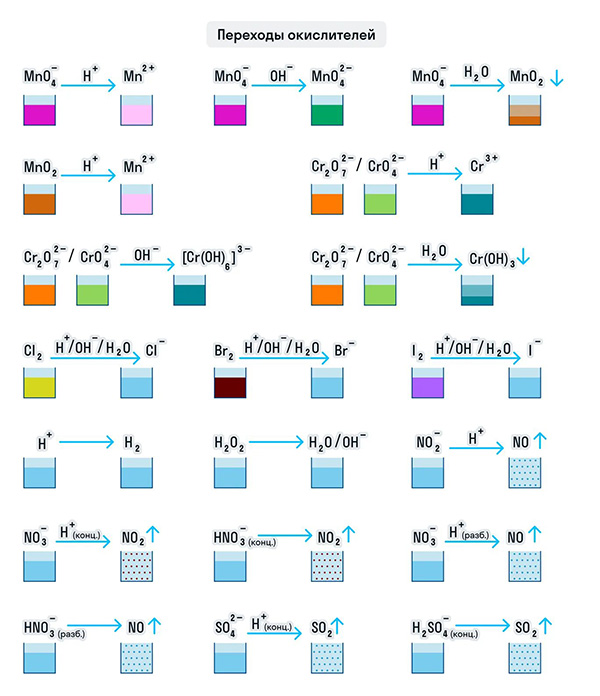
В зависимости от среды проведения реакции Mn +7 и Cr +6 ведут себя по-разному. Рассмотрим на схемах:
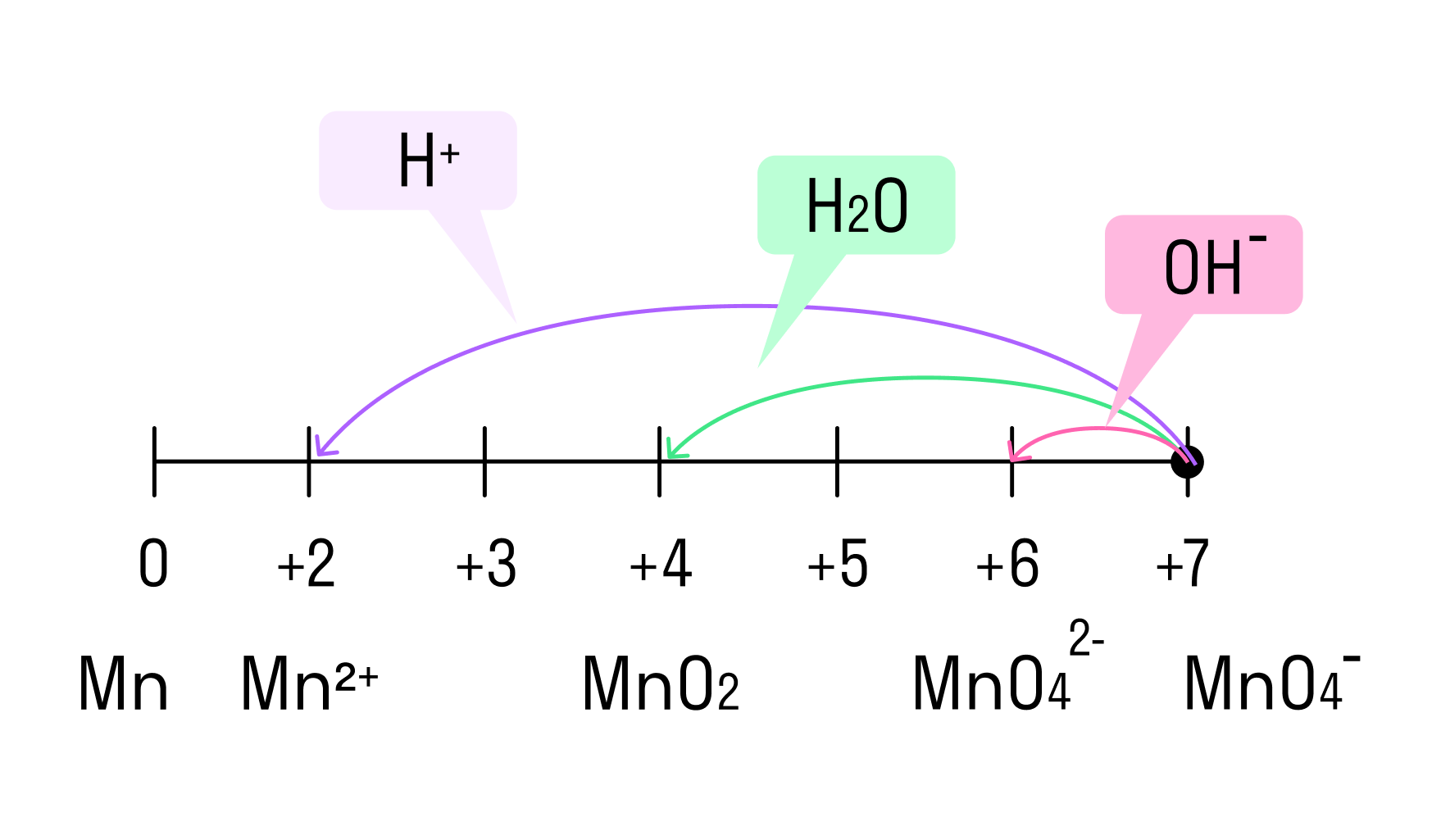
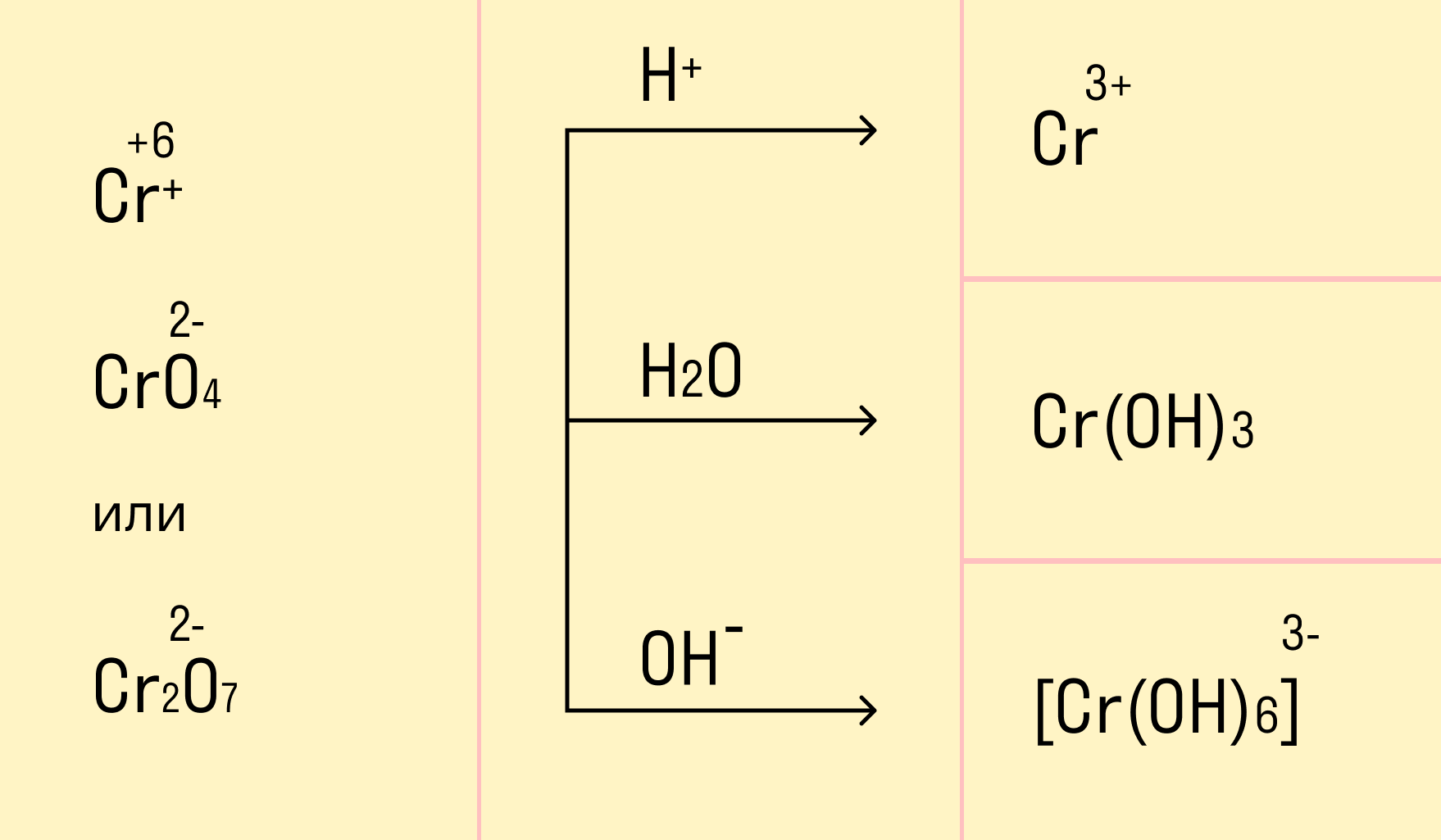
И марганец, и хром в кислой среде (H + ) образуют соли той кислоты, которая образовывала среду. В нейтральной среде (H2O) марганец превращается в оксид бурого цвета, а хром — в серо-зеленый нерастворимый в воде гидроксид. В щелочной среде (OH − ) марганец превращается в манганат (MnO4 2− ), а хром — в комплексное соединение светло-зеленого цвета.
Только окислителями могут быть простые вещества-неметаллы. Например, представители VIIA группы — галогены. Проявляя окислительные свойства в кислой среде, галогены восстанавливаются до соответствующих им галогеноводородных кислот: HF, HCl, HBr, HI. В щелочной среде образуются соли галогеноводородных кислот.
Кислород превращается в анион с устойчивой степенью окисления −2. А сера ведет себя как окислитель по отношению к водороду и металлам, образуя при этом сероводород и сульфиды.
Только окислителями могут быть и протон водорода (H + ) и катионы металлов в их высших степенях окисления при нескольких возможных. Ион Н + при взаимодействии с восстановителями переходит в газообразный водород (H2), а катионы металлов — в ионы с более низкой степенью окисления: 2CuCl2 + 2KI = CuCl + 2KCl + I2.
Рассмотрим как ведут себя сильные кислоты-окислители — азотная и серная. В зависимости от их концентрации меняются и продукты реакции.
Разбавленная азотная кислота никогда не реагирует с металлами с выделением водорода в отличие от разбавленной серной кислоты. Обе эти кислоты реагируют с металлами, стоящими в ряду активности после водорода.
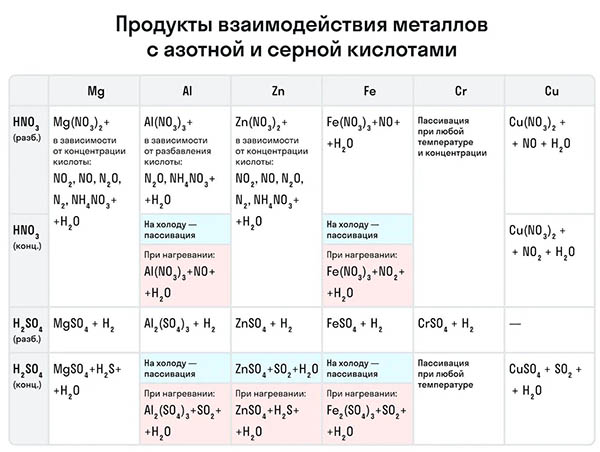
Эти кислоты проявляют окислительные способности и с некоторыми неметаллами, окисляя их до соответствующих кислот в высшей степени окисления неметалла-восстановителя.
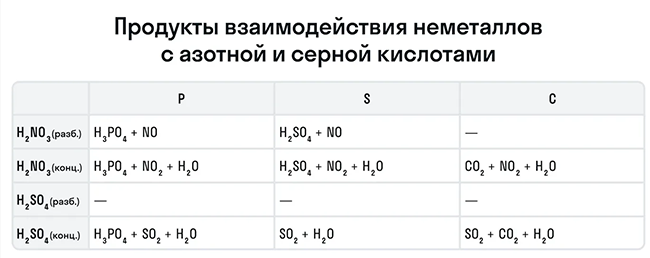
Для удобства мы собрали цвета переходов важнейших веществ-окислителей в одном месте.
Примеры веществ-восстановителей
Типичными восстановителями могут быть щелочные (IA) и щелочноземельные (IIA) металлы, цинк и алюминий, а также катионы металлов в своих низших степенях окисления при нескольких возможных. Например:
Типичными восстановителями также могут быть бескислородные кислоты и их соли. Например, H2S + 4Cl2 + 4H2O = 8HCl + H2SO4.
Гидриды активных металлов (щелочных и щелочноземельных) тоже являются типичными восстановителями. Например, NaH + H2O = NaOH + H2.
Для удобства мы собрали цвета переходов важнейших веществ-восстановителей в одном месте.

Пошаговый гайд от Екатерины Мурашовой о том, как перестать делать уроки за ребёнка и выстроить здоровые отношения с учёбой.

Окислительно-восстановительная двойственность
Окислительно-восстановительная двойственность — это способность атома проявлять как свойства окислителя, так и свойства восстановителя в зависимости от условия протекания химической реакции.
Разберем вещества, атомы которых обладают окислительно-восстановительной двойственностью.
По отношению к водороду и металлам сера играет роль окислителя: S + H2 = H2S.
При взаимодействии с сильными окислителями повышает свою степень окисления до +4 или +6: S + KMnO4 = K2SO4 + MnO2.
Кислородсодержащие соединения серы в степени окисления +4
Сера в сульфитах и сернистой кислоте при взаимодействии с сильными окислителями повышает степень окисления до +6: SO2 + 2HNO3 (конц) = H2SO4 + 2NO2.
С восстановителями соединения серы проявляют окислительные свойства, восстанавливаясь до степени окисления 0 или −2: SO2 + C = CO2 + S.
Пероксид водорода
Атом кислорода в пероксиде водорода находится в промежуточной степени окисления –1, и в присутствии восстановителей может понижать степень окисления до –2: 4H2O2 + PbS = PbSO4 + 4H2O.
Атом кислорода в пероксиде водорода находится в промежуточной степени окисления –1, и в присутствии окислителей может повышать степень окисления до 0: 3H2O2 + 2KMnO4 = 3O2 + 2MnO2 + 2KOH + 2H2O.
Простое вещество йод
Окислительная способность проявляется у йода в реакции с такими восстановителями, как сероводород, фосфор и металлы: I2 + H2S = S + 2HI.
Йод при взаимодействии с более сильными окислителями играет роль восстановителя: I2 + 5Cl2 + 6H2O = 2HIO3 + 10HCl.
Азотистая кислота и нитриты
При взаимодействии с более сильными окислителями азот повышает степень окисления до +5 и превращается либо в азотную кислоту из азотистой, либо в нитрат-анион из нитрит-аниона: 5NaNO2 + 2KMnO4 + 3H2SO4 = 5NaNO3 + 2MnSO4 + K2SO4 + 3H2O.
При взаимодействии с сильными восстановителями обычно происходит восстановление до NO (иногда до других соединений азота в более низких степенях окисления): 2HNO2 + 2HI = 2NO + I2 + 2H2O.
Для удобства мы собрали представителей типичных окислителей и восстановителей в одну схему.

Классификация окислительно-восстановительных реакций
Окислительно-восстановительные реакции можно поделить на четыре типа:
Рассмотрим каждую по отдельности.
Межмолекулярная ОВР — это реакция, окислитель и восстановитель которой являются различными веществами.
2KI + Br2 = 2KBr + I2, где Br2 — окислитель, а KI — восстановитель (за счёт I −1 ).
Внутримолекулярная ОВР — это реакция, в которой один атом является окислителем, а другой восстановителем в рамках одного соединения.
Пример такой окислительно-восстановительной реакции:
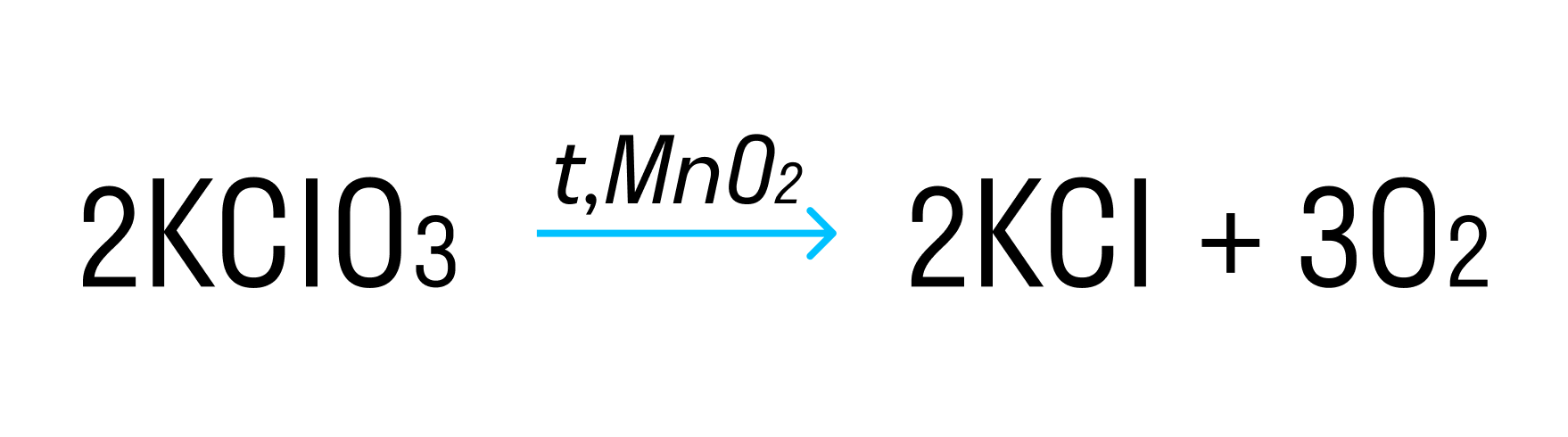
где Cl +5 — окислитель, а O −2 — восстановитель.
Термическое разложение нитратов — это внутримолекулярная ОВР. Вот схема разложения нитратов в зависимости от металла, входящего в состав соли.
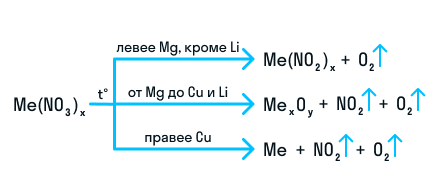
Исключение — разложение нитрата железа (II): 4Fe(NO3)2 = 2Fe2O3 + 8NO2 + O2. Здесь железо окисляется до +3 вопреки правилам. Иначе разлагается при нагревании и нитрат аммония: NH4NO3 = N2O + 2H2O.
Окислительно-восстановительная реакция диспропорционирования — это реакция, в ходе которой один и тот же атом является и окислителем, и восстановителем. Например, 3HNO2 = HNO3 + 2NO + H2O, где N +3 переходит в N +5 , являясь восстановителем, и N +3 переходит в N +2 , являясь окислителем.
Окислительно-восстановительная реакция контрпропорционирования — это реакция, в которой атомы одного и того же химического элемента в разных степенях окисления входят в состав разных веществ, при этом образуя новые молекулы одного и того же продукта.
Основные правила составления ОВР
Подобрать среди исходных веществ окислитель и восстановитель, а также вещество, которое отвечает за среду — при необходимости. Для этого нужно расставить степени окисления элементов и сравнить их окислительно-восстановительные свойства.
Составить уравнение реакции и записать продукты реакции. Следует помнить, что в кислой среде образуются соли одно-, двух- и трехзарядных катионов, а для создания среды чаще всего используют серную кислоту. В кислой среде невозможно образование оснóвных оксидов и гидроксидов, так как они вступят в реакцию с кислотой. В щелочной среде не могут образовываться кислоты и кислотные оксиды, а образуются соли.
Уравнять методом электронного баланса или методом полуреакций.
Составим алгоритм для уравнивания окислительно-восстановительных реакций методом электронного баланса.
Главное условие протекания ОВР — общее число электронов, отданных восстановителем, должно быть равно общему числу электронов, принятых окислителем.
Определите атомы, которые меняют свои степени окисления в ходе реакции.
Выпишите, сколько электронов принял окислитель и отдал восстановитель. Если восстановителей несколько, выписываем все.
Найдите НОК для суммарно отданных/принятых электронов.
Расставьте первые полученные коэффициенты перед окислителем и одним или несколькими восстановителями.
Уравняйте все присутствующие металлы в уравнении реакции.
Уравняйте кислотные остатки.
Уравняйте водород — в обеих частях его должно быть одинаковое количество.
Источник: skysmart.ru